3 Lü Antibiyotik

ADO Klinik Bilimler Dergisi
Diş Hekimliğinde Üçlü Antibiyotik Patın Kullanımı
Yazarlar: Abidin T MUTLUAY, Merve MUTLUAY
Cilt 8 , Sayı 2 , 2017 , Sayfalar 1561 - 1570
Konular:-
Anahtar Kelimeler:Kanal tedavisi,Immatür dişler,Üçlü antibiyotik pat
Özet: Kök kanallarından bakterilerin elimine edilmesi endodontik tedavilerin temel amacıdır. Kök kanallarının karmaşık anatomisi nedeniyle, mekanik enstrümantasyon kanal duvarlarındaki patojen mikroorganizmaların elimine edilmesinde yeterli değildir. Bu nedenle, mekanik preparasyona ek olarak endodontik irriganlar ve medikamanlar kök kanal sistemindeki bakteri miktarının azaltılmasında, böylece iyileşmesini sağlamasında önemli yer tutmaktadır. Endodontik enfeksiyonların polimikrobiyal yapıda olması nedeniyle, uygulanacak medikamanın antibakteriyel ilaçların kombinasyonundan oluşması yararlı olabilir. Üçlü antibiyotik pat olarak tanımlanan metronidazol, siprofloksasin ve minosiklin karışımı enfekte kök dentininin sterilizasyonunda etkilidir. Bu makalede, üçlü antibiyotik karışımının genel özellikleri, antibakteriyel etkinliği, uygulama alanları, doku reaksiyonu ve dezavantajları incelenmektedir
ATIFLAR
Atıf Yapan Eserler
KAYNAK GÖSTER
BibTex
@article{2017, title={Diş Hekimliğinde Üçlü Antibiyotik Patın Kullanımı}, volume={8}, number={1561–1570}, publisher={ADO Klinik Bilimler Dergisi}, author={Abidin T MUTLUAY,Merve MUTLUAY}, year={2017} }
APA
Abidin T MUTLUAY,Merve MUTLUAY. (2017). Diş Hekimliğinde Üçlü Antibiyotik Patın Kullanımı (Vol. 8). Vol. 8. ADO Klinik Bilimler Dergisi.
MLA
Abidin T MUTLUAY,Merve MUTLUAY. Diş Hekimliğinde Üçlü Antibiyotik Patın Kullanımı. no. 1561–1570, ADO Klinik Bilimler Dergisi, 2017.
Helico Bakter Pilori ve Tedavisi
 Türkiye’de 2014’de Helikobakter Pylori (HP) Tedavisi Nasıl Olmalıdır?
Türkiye’de 2014’de Helikobakter Pylori (HP) Tedavisi Nasıl Olmalıdır?Prof. Dr. Ahmet UYGUN
Helikobakter pilori (HP) dünyadaki en yaygın infeksiyon etkenidir. HP enfeksiyonun tedavisindeki amaç, mikroorganizmayı tamamen elimine etmektedir. HP enfeksiyonu için ideal tedavi, sürekli olarak; ≥% 95 gibi yüksek şifa oranı olan ve hastalar tarafından iyi tolere edilen bir tedavidir. Ancak henüz böyle bir tedavi yoktur. HP eradikasyonunda kullanılan tedavi ile en az % 80 –85 olguda eradikasyon sağlanmalıdır. Bu kabül edilebilir bir orandır. Arzu edilen eradikasyon oranı ise %90 ve üstü olmalıdır (1,2). Bu nedenle birinci basamakta etkinliği kanıtlanmış tedavi protokollerinin kullanılması önemlidir. Çünkü birinci basamak tedavisinde başarısızlık gözlenirse 2’ci ve 3’cü basamak tedavilerde başarı oranı daha da düşüktür. Uygun ve etkili olmayan tedavi rejimleri HP’nin direnç kazanmasına, sonuçta toplumda dirençli HP suşlarının yayılmasına yol açarlar.
HP enfeksiyonunun tedavisindeki ana engel, ilaçlara uyumun kötü olması ve HP’ya karşı direnç gelişmesidir. HP enfeksiyonunun tedavisi için ideal bir ilaca maalesef bugün için sahip değiliz. Fakat HP’ye etkili elimizde bir çok ilaç mevcuttur. Bu ilaçlardan iyi bir kombinasyon yapılıp ve uygun süre kullanılırsa% 90’ın üzerinde bir başarıyla Hp’yi eradike etmek mümkündür.
HP için ideal tedavide aranan özellikler şunlardır:
1- Ucuz olmalı
2- % 90 - 95’in üzerinde eradikasyon sağlamalı
3- Kullanımı kolay olmalı
4- Kullanan kişide rahatsızlık oluşturmamalı ve ciddi yan etkinin olmamadır.
HP’ye karşı etkili bir ilacın sahip olması gereken özellikler şunlardır:
1- In vitro HP’ye karşı etkili olmalı
2- In vitro yavaş çoğalan-büyüyen coccoid formdaki HP’ye karşı etkili olmalı
3- Edinilmiş (sekonder) dirence yol açmamalı
4- Minimal lokal ve sistemik yan etkiye sahip olmalı
5- İntragastrik aktiviteye sahip olmalı, hızlı çözülmeli ve midede yayılmalı
6- Mide mukozasını lokal olarak geçebilmeli
7-Mide lümeninde ve mukus tabakasında farklı PH’larda, hem stabil hem de aktif olabilmeli
8- Sistemik dolaşımdan mide mukozasına ve mukusa geçebilmeli (1).
HP infeksiyonunun eradikasyon endikasyonları ve bunun nasıl yapılacağı ile ilgili tartışmalar; özellikle 1’ci basamak sağlık hizmetlerinde devam etmektedir.
Bu karışıklıkları önlemek için, Avrupa Helicobacter Pylori Çalışma Grubu (EHPSG) tarafından ilk kez 1997 yılında, sonuncusu 2005’de yapılan uzlaşı toplantıları ile, Maastrich 3-2005 Konsensüs raporu adıyla yayınlanmıştır.
Bu son uzlaşı toplantısında;
- Kimleri tedavi edeceğiz?.
- Nasıl tanı konulacak?
- Nasıl tedavi edilecek?. Soruları üzerinde fikir birliği oluşturulmuştur (3).
Kimleri Tedavi edeceğiz ?
HP ile enfekte insanların % 100’de histopatolojik olarak gastritis olduğu halde çoğu asemptomatiktir. HP ile enfekte olan yetişkinlerin yaklaşık %30’da dispeptik semptomlar vardır. Dispeptik yakınmaları olanlarında yaklaşık %20’de peptik ülser, %1-2’de mide kanseri olma riski vardır. Dispeptik semptomlarla baş vuran tüm hastalara HP testi yapılmalıdır. Alarm semptomları varsa veya yaşı 40’ın üzerinde ise endoskopi dahil tüm inceleme yapılmalıdır.
Hastaya endoskopi düşünülmüyorsa HP için non-invaziv testlerden Üre Nefes testi veya HP gaita antijen testi yapılmalıdır. Her ikisi de aktif enfeksiyonun varlığını gösterir. Hasta daha önce HP’ye yönelik tedavi görmemişse Anti- HP- IgG serolojik testi de yapılabilir. Bu test mevcut veya geçirilmiş enfeksiyonu gösterir.
HP testi pozitif çıkınca eradikasyon düşünüyorsanız o zaman HP testi yapınız. Çünkü HP pozitif olgularda eradikasyon tedavisi yapılmalıdır. Asemptomatik olgularda HP testi yapmak doğru değildir. Test sonucu pozitif çıkan hastaları tedavi etmemek etik değildir.
Tedavi önerisi yapılırken tavsiyeler 3 düzeyde değerlendirilmektedir:
- Kuvvetle tavsiye edilen
- Tavsiye edilen
- Kesin değil, önerilebilir, olarak ayrılmıştır.
Bu tavsiyeler ile ilgili bilimsel deliller 5 seviyede toplanmıştır. Bunlar;
- İyi tasarlanmış ve uygun şekilde kontrollü çalışmalar
2- İyi tasarlanmış, herhangi bir insan topluluğunda yada vaka kontrollü çalışmalar, indirekt delillerle desteklenmiş kusursuz çalışmalar
3- Vaka raporları, ciddi şekilde planlı indirekt olarak ima eden deliller
4- Klinik tecrübeler
5- Fikir oluşturmak için yeteli delil olmaması
Maastrich 3-2005 Konsensüs raporuna göre, HP eradikasyon tedavisi vereceğimiz endikasyonlar şunlardır (3,4).
Kuvvetle tavsiye edilen endikasyonlar : Bilimsel Delil Seviyesi
- DÜ veya GÜ ( aktif veya komplikasyon içermeyen) 1
- MALT-lenfoma (Mide de) 2
- Atrofik gastritis 2
- Daha önce mide ameliyatı olanlar 3
- Birinci derecede ailesinde mide kanseri hikayesi olanlar 3
- Hasta bizzat kendisi Hp için tedavi arzu ediyorsa 4
Tavsiye edilen endikasyonlar ve ilgili durumlar: Bilimsel Delil Seviyesi
1- Dispepsi’li hastalar 2
2- GÖRH 3
3- NSAİİ 2 -1
4- İdiopatik trombositopeni (İTP) 3 - 4
5- Açıklanamayan Demir eksiliği anemisi (DEA) 3-4
6- Diğer tartışmalı ekstra gastrik ( İKH, Serebro Vasküler Aksedan , Kronik Bronşit, Astım, KOAH, Kronik idiopatik Nötropeni, Safra kesesinde kolesterol taşı oluşumu, İBH, Kolorektal Kanser, Kolonun Adenomatöz Polibi, İdipatik Anteriör Üveit, Blefaritis, Otitis Media, İdipatik Urtiker, Çoçuklarda otoimmün troit hastalığı, Tekrarlayan aftöz stomatit, Glossitis, Halitosis, Lingual hiperplazi, Plazma Gherelin dinamiklerini etkileyerek, nöroendokrin, nörotoksinleri ve dopaminerjik nöronları etkileyerek parkinsonizmi hızlandırma) endikasyonlar (4).
1- Dispepsi’li Hastalar ve HP :
Dispepsi’li hastaların tedavisi ile ilgili karar verirken hastaları;
- Alarm semptomu olanlar,
- Araştırılmış hastalar,
- Araştırılmamış hastalar olarak 3’e ayırmak, tedavide kolaylık sağlayacaktır.
Alarm semptomu olan hastalar kesin olarak tedavi edilmelidir.
Alarm semptomları :
- 40 yaşın üstünde olmak
- Semptomların yakın zamanda ortaya çıkması
- Semptomların ciddi-ağır olması
4- Klinik olarak organik hastalık şüphesi (ülser, kanser, vs.) Ateş , Anemi, Kilo kaybı, Yutma güçlüğü, Tekrarlayan kusma, Karındaki kitle tespiti
- Ailesel kanser hikayesi
- Tedaviye cevapsızlık
- Hastanın kanser endişesi taşıması
- Hastanın daha önce tetkik edilmemiş olması
2- Gastroözefagial Reflü Hastalığı (GÖRH) Olanlar ve HP :
HP infeksiyonu ile GÖRH arasındaki ilişki hala tartışmalıdır. Bazı araştırmacılar GÖRH ve onun komplikasyonları konusunda HP’nin koruyucu rolü olduğunu ileri sürmüşlerdir. Fakat diğerleri bu bulguları doğrulamamıştır. GÖRH için uzun süreli anti-sekretuvar tedavi gerektiği zaman HP eradikasyonu tavsiye edilmektedir. Çünkü asit salgısının uzun süre baskı altına alınmasının, midenin fundus bölümünde HP etkisiyle atrofik gastrit gelişmesini hızlandırdığı düşünülmektedir. Ne olursa olsun HP infeksiyonunun mevcut olup olmadığının araştırılması ve mevcutsa, asit salgısının uzun süreli olarak baskı altına alınmasından önce, HP’nin ortadan kaldırılması önerilmektedir. HP’nin bilinen herhangi bir faydası olmadığından bu bakterinin eradikasyonunu ile diğer gastroduoenal komplikasyonlara ait bir risk faktörüde uzaklaştırılmış olacaktır (8).
3- HP ve NSAİİ Kullananlar :
HP ve NSAII’ler / aspirin, peptik ülser gelişmesi ve peptik ülser kanaması konusunda bağımsız risk faktörleridir. NSAII’leri bu bakımdan aspirinden ayırt etmek gerekir.
HP eradikasyonu NSAII kullanımına başlanmadan önce yapıldığında peptik ülser ve buna eşlik eden semptomların sıklığını azaltır. HP eradikasyonu, antisekretuvar tedavi uygulanan, ancak NSAII kullanmaya da devam eden hastalarda mide veya duodenum ülserinin iyileşmesini hızlandırmaz. NSAII kullanmaları nedeniyle yüksek risk altında olan hastalardaki HP eradikasyonu, ülserlerin tekrar kanamasının önlenmesinde etkisizdir ve bu nedenle de söz konusu hastalarda uzun süreli proton pompası inhibisyonuna ihtiyaç vardır (13).
Bu konuda literatürde, birbirini tutmayan verilerin söz konusu olduğu, karmaşık bir konudur. Ancak daha sonra gelişebilecek peptik ülserin ve dispeptik semptomların açıklanmasında karışıklığa yol açabilecek bir faktörü ortadan kaldırmak amacıyla, NSAII tedavisi planlanan hastalarda HP eradikasyonu yapılmalıdır. Peptik ülser anamnezi veren ve düşük dozda aspirin tedavisi altında olan hastalarda, HP testi yapılması ve pozitif olanlarda eradikasyon yapılmalıdır (14).
Clopidogrel GİS kanama riskini artırmaktadır. Bu durumda HP’nin rolü değerlendirilmemiştir. Serebro vasküler hastalıkta sinerjik etki ile yarar sağlayan Aspirin ve Clopidogrel kombinasyon tedavisinde daha ileri çalışmalara ihtiyaç vardır .
Ülseri iyileşmiş ve aspirine bağlı ülser kanama anamnezi olan hastalarda, tekrarlayan ülser kanamalarını önlemede, aspirin ve PPI, clopidogrel’den daha üstündür. Bu günkü tavsiye, sadece aspirine karşı GİS uyumsuzluğu olan hastalarda clopidogrel verilmelidir. Ancak bu ispatlanmamıştır (15, 16,17).
HP ve COX-2 inhibitörleri arasındaki ilişki önemli idi. Fakat bu ilaçların yan etkileri nedeniyle tüm çalışmalar durdurulmuştur.
4- İdiopatik Trombositopeni (İTP) :
Literatürler incelendiğinde ITP’li hastaların %58’nin HP ile infekte olduğu görülmektedir. ITP’li hastalarda HP eradikasyonu yapılınca trombosit sayısında önemli bir artış gözlenmiştir.
Eradikasyon tedavisi vakaların yaklaşık yarısında kısmi veya tam olarak trombosit sayısında artış yapmıştır. Bu trombosit yüzeyindeki antijenik çapraz reaksiyonu ile ilgilidir. Bu konunun plesabo kontrollü çalışmalar ile desteklenmeye ihtiyacı vardır (3,18-19).
5- Açıklanamayan Demir Eksiliği Anemisi (DEA) :
HP gastriti ile açıklanamayan demir eksiliği anemisi arasında, ilişkinin olduğu giderek artmaktadır .
Diğer Tartışmalı Ekstra Gastrik Endikasyonlar :
HP ile mide dışındaki sistemlerle ilgisini araştırmak için bir çok sistemde araştırma yapılmıştır. Ancak bunlarla ilgili olarak kesin bir sonmuca varmak için çok erkendir. Bazı yayınlar lehte bazı yayınlar ise ilgisiz sonuçlara varmışlardır.
İskemik kalp hastalığı, Serebro Vasküler Aksedan , Kronik Bronşit, Astım, KOAH, Kronik idiopatik Nötropeni, Safra kesesinde kolesterol taşı oluşumu, İnflamtuvar barsak hastalığı, Kolorektal Kanser, Kolonun Adenomatöz Polibi, İdipatik Anteriör Üveit, Blefaritis, Otitis Media, İdipatik Urtiker, Çoçuklarda otoimmün troit hastalığı, Tekrarlayan aftöz stomatit, Glossitis, Halitosis, Lingual hiperplazi, Plazma Gherelin dinamiklerini etkileyerek, nöroendokrin, nörotoksinleri ve dopaminerjik nöronları etkileyerek parkinsonizmi hızlandırma hızlandırdığı tespit edilmiştir. Bu konuda karşılaştırmalı ileri araştırmalara ihtiyaç vardır (4, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30).
Nasıl tanı konulacak?
HP infeksiyonunun ilk basamak sağlık hizmetlerinde teşhisi için, üre nefes testi (ÜNT) veya dışkıda antijen arayan test uygulanması şiddetle önerilmektedir. HP eradikasyon tedavisi sonrasında ilk uygulanacak test üre nefes testi’dir. Bu test yoksa, dışkıda antijen arayan test kullanılabilir.
İlk basamak sağlık hizmetlerinde “test et ve tedavi et” stratejisinin uygulanabilmesi için, HP infeksiyonunun non-invazif yöntemlerle teşhis edilmesi gerekir. UNT ve dışkıda antijen arayan testler bu amaçla tercih edilir.
Hastaya endoskopi düşünülmüyorsa HP için non-invaziv testlerden Üre Nefes testi veya HP gaita antijen testi yapılmalıdır. Her ikisi de aktif enfeksiyonun varlığını gösterir. Hasta daha önce HP’ye yönelik tedavi görmemişse Anti Hp IgG serolojik testi de yapılabilir. Bu test mevut veya geçirilmiş enfeksiyonu gösterir. Serolojik test hariç, PPI kullanılması tüm testler için yalancı negatifliğin bir kaynağıdır. Testten iki hafta önce PPI kesilmelidir.
Nasıl tedavi edilecek?.
HP enfeksiyonun tedavisindeki amaç mikroorganizmayı tamamen elimine etmektedir. Bu nedenle günümüzde HP’ye etkili antibiyotiklerin yanı sıra mide asit sekresyonunu inhibe eden ajanlar da kullanılmaktadır. Maalesef günümüzde HP’yi eradike edecek tek antibiyotik yoktur. Yan etkiye sahip olmayan, rezistans geliştirmeyen ideal antibakteriyel ajana bugün sahip değiliz.
HP İnfeksiyon eradikasyonunda ilk seçenek tedavi (First-line therapies) Maastrich-3 2005 uzlaşı raporundaki tavsiye; hala PPİ + Klaritromisin + Amoksisilin yada Metronidazol ile kombinasyonunu içeren üçlü tedavdir.
Birinci basamak tedavide bu rejimin bir-iki hafta süreyle kullanılmasının efektif olduğu ve eradikasyon oranlarının % 75-90 arasında değiştiği bildirilmektedir. Ülkemizde, malasef aynı kombinasyon, değişik bölgelerde yapılan çalışmalarda, eradikasyon oranını yaklaşık olarak % 45-60 arasında bulunmuştur.
Tedavi başarısızlığındaki ana neden antibiyotik direncidir. Rezistans oranları bölgelere göre çok farklılık göstermektedir.
Bugün için ABD’de HP suşlarının % 12’si Clarithromyscin’e rezistandır. Bu Almanyada %9.8, İtalyada % 26.7’dir. Türkiyede %25-40 seviyesindedir.
Gelişmiş batı ülkelerinde Metranidazol’e karşı HP’deki mevcut rezistans % 10-50 sıklıktadır. Gelişmete olan ülkelerde ise HP suşlarında metranidazole rezistans % 80-90’lara ulaşmaktadır. HP’nin Amoxicilline ve Tetracycline’e karşı nadirde olsa rezistans geliştirdiği bilinmektedir (31, 32,33, 34,35).
Eradikasyon oranları % 80’nin altına düşen bölgelerde alternatif tedavi yaklaşımları önerilmektedir (31). Bunlar;
- Tedavi süresinin uzatılması
- Dörtlü tedaviler
- Ardışık tedaviler
- Adjuvant tedavi
5- Farklı antibiyotiklerin (Furazolidon, Tinidazol, Levofloksasin) bulunduğu protokolleri içeren tedavi şemaları (36).
Üçlü tedavinin süresi konusunda tartışma halen devam etmektedir. Bazı araştırıcılar 7-10 günlük bir süreyi uygun görürken diğerleri en uygun sürenin 14 gün olduğunu kabul etmektedir. Üçlü tedavi 2 hafta yapılırsa eradikasyon oranı 7 günlük tedaviden % 7-9 daha iyidir (31, 36).
Dörtlü tedaviler (PPI, Bizmut, tetrasiklin ve metranidazol)’le özellikle yaşlılarda memnuniyet verici oranlar elde edilmiştir (37).
Ardışık tedavi şemaları ile ( 14 gün PPI, ilk 7 gün amoksisilin, 8-14 günler metronidazol , tetrasiklin)’le % 90 üstünde eradikasyon oranları gözlenmiştir Klaritromisine resistan hastalarda, İtalyan grubu ardışık (sequential) tedavi ile 7 gün PPI, Amoxicilin takiben 7 gün PPI, Tetrasiklin, Medranidazole ile %90 üstü bir eradikasyon sağlamışlardır. (38).
Ülkemizde kliniğimizce yapılmış araştırmada aynı protokolle, eradikasyon oranı ancak % 80.1 bulunmuştur (39).
Adjuvan tedavi ve farklı antibiyotikler ile eradikasyon oranları artırılmaya çalışılmış, ancak umulan sonuç alınamamıştır. Bovine lactoferrin ile yapılan adjuvan tedavide HP koloni oranını azaltmakta , Fakat tam eradikasyon sağlamamaktadır. Sonuçlar tartışmalıdır. Farklı antibiyotiklerin (Furozolidon, Tinidazol, Levofloksasin) bulunduğu protokoller genelde 2’ci basamakta kullanılmakta fakat eradikasyon oranı düştükçe bu antibiyotikler 1’ci basamak tedavide kullanılmaktadır (40, 41,42).
Tedavi seçiminde basit bir kural olarak, Batı toplumlarında, penisilin allerjisi olan olgularda bizmut dörtlü tedavinin, penisilin allerjisi olmayan olgularda klaritromisin tabanlı üçlü tedavinin seçilmesi göz önünde bulundurulması önerilmektedir. Ancak bu tedavi ile eradikasyon oranı ortalama % 50 olan ülkemizde kullanılmamalıdır.
Kullanılan rejimlerde amoksisilin, ampisilin ile, tetrasiklin, doksisiklin ile ve klaritromisin, eritromisin ile değiştirilmemelidir.
Ayrıca antibiyotik kombinasyonunda şu noktalar dikkate alınmalıdır;
Bakterinin DNA ve RNA yapısını etkileyip, nükleik asit sentezini bozarak etkili olan, Kinolonlar (ciproxin, levofloxacin, moxifloksasin), Nitroimibazoller (metronidazol), Rifampisin aynı grupta yer almamalıdır.
Bakterinin ribozom fonksiyonunu bozarak etkili olan Tetrasiklinler ile Makrolid grubu (clarithromycin, erithromycin, azithromycin) antibiyotikler aynı grupta yer almamalıdır.
Hücre duvar sentezini bozan penisilinler ile Ribozomal fonsiyonu bozan tetrasiklinler mümkünse bir arada kullanılmamalıdır. Çünkü tetrasiklin protein sentezini inhibe ettiği için penisilinlerin antibakteriyel etkinliğini antagonize etmektedir. HP eradikasyonunda yapılan çalışmalarda invitro olarak antibakteriyel etkide azalma olmadığı, fakat invivo olarak bu iki ilaç kombinasyonunun eradikasyonda düşük oranda tespit edilmesi nedeniyle HP tedavisinde kullanılmaması önerilmektedir.
Proton pompa inhibitörlerinin üçlü tedavide birbirlerinden etkinlik yönünden farklılığı yoktur.
Omeprazole 20 mg, Lansoprazole 30 mg, Rabeprazole 20 mg, Esomeprozole 40 mg, Pantoprazole 40 mg günde iki kez kullanılmalıdır.
Clarithromycine 500 mg günde iki kez, Amoxicilline 1 gram günde iki kez, Ranitidine bismuth citrate 400 mg günde iki kez, Bismuth subsitrate 300 mg günde dört kez, Metranidazole 500 mg günde üç kez, Tetracycline 500 mg günde dört kez kullanılmalıdır.
Bazı araştırmacılar üçlü tedavilerde Proton pompa inhibitörlerini yada bizmut tuzlarını üçlü tedavi tamamlandıktan sonra 2 hafta daha devam etmeyi önermektedir.
Ranitidine Bizmuth Citrate ile yapılan üçlü tedavilerde antibiyotik rezistansı daha az gelişir. PPI’lı üçlü tedavilerde eradikasyon sonuçlarının klaritromisin rezistansı nedeniyle düşük olması sebebiyle ülkemizde ilk seçenek tedavinin Ranitidine Bizmuth Citrat’lı üçlü tedavi olması yada PPI, Bismuth subsitrate, Tetracycline, Medranidazole 4’lü kombinasyonu önerilmektedir.
Birinci basamakta ayrıca, PPİ, Amoxicilin, Levofloksasin ve PPİ, Clarithromycine, Tinidazol kombinasyonlarıda kullanılabilir.
PPI , Clarithromycine , Medranidazole kombinasyonu, PPI , Clarithromycine , Amoxicilline kombinasyonununa oranla daha iyi bir eradikasyon oranı sağlamaktadır.
Ancak PPİ, Clarithromycine ve Metronidazol tedavisi alan ve kür sağlanamayan hastalarda HP’nin hem klaritromisine hem de metronidazole direnç kazanabileceğinin önemi hatırlanmalı ve kurtarma tedavilerinde seçeneklerin azaltılmaması için bu rejimin penisilin alerjisi olan yada bizmut dörtlü tedaviyi tolere edemeyen olgulara saklanması önerilmektedir.
Öte yandan 2009 yılındaki yayınlarda, 1ci basamakta kullanılan ardışık tedavi ile ilgili ciddi eleştiriler yapılmıştır. Gerek hasta uyumu gerekse hastaya anlatmak için çeşitli sorunlar yaşandığı vurgulanmıştır ve bu durumdaki hastalara “concomitan” bitişik tedavi önerildi (43). Bu tedavinin Türkiye’deki başarı oranı çalışma yapılmadığı için belli değildir.
Sonuç olarak tedavi endikasyonu doğru konulmuş bir Hp enfeksiyonunda izlenecek yol ve kullanılabilecek seçenekler şunlardır :
Birinci Basamak Tedavide:
Ülkemizde klasik 3’lü tedavi kullanılmamalıdır. Bu nedenle 1ci basamakta bu tedavi başarısız gibi kabül edilerek tedavi şenenekleri düşünülmelidir.
A- Şayet kültür yapılamayacak bir ortam yada kurumda çalışıyor iseniz ve klaritromisin direnci %20den fazla olduğunu biliyor iseniz 14 gün süre ile;
1- PPI 2x1 + Amoksisilin 1gr 2x1 + Metronidazol 500mg 3x1 yada
2- PPI 2x1 + Klaritromisin 500mg 2x1 + Metronidazol 500mg 3 x1( birinci basamakta tercih edilmiyor)
3- PPI 2x1 + Amoksisilin 1gr 2x1 + Tetrasiklin 500mg 4x1 + Bizmut subsitrat 300mg 4x1 veya Metronidazol 500mg 3x1 yada
4- PPI 2x1+ Amoksisilin 1gr 2x1 + levofloksasin 500 mg 1x1 ( tercih edilmiyor)
5- Ardışık tedavide PPI 2x1 + Amoksisilin 1gr 2x1 / 7 gün takiben 8-14cü günlerde PPI + Tetrasiklin 500mg 4x1 + Metronidazol 500mg 3x1 yada
6- “Concomitan” birlikte yada aynı zamanda olarak adlandırılan PPI 2x1+ Amoksisilin 1gr 2x1 + Tetrasiklin 500mg 4x1 + Metronidazol 500mg 3x1 yada Tetrasiklin yerine Klaritromisin konulması ile elde edilen PPI + 3 antibiyotikten oluşan kombinasyon kullanılabilir.
7- PPI 2x1 + Amoksisilin 1gr 2x1 + Furazolidan 200mg 2x1 (Türkiyede tablet formu yok. TC sağlık bakanlığı vasıtası ile getirtilebilir)
8- PPI 2x1+ Amoksisilin 1gr 2x1 + Tinidazol 500mg 2x1 (Türkiyede yok. TC sağlık bakanlığı vasıtası ile getirtilebilir)
B- Şayet kültür yapılabilecek bir ortam yada kurumda çalışıyor iseniz;
Hp’ye karşı antibiyotik duyarlılık testi yapılmalı sonuca göre tedavi planlanmalıdır.
Sonuç ve Öneri
- Klasik 3’lü tedavi ülkemizde etkisizdir. Ancak;
- Bizmut,
- Probiyotik,
- C ve E Vitaminleri eklenebilir.
- Bizmutlu 4’lü tedaviyi 1.ci basamakta daha sık kullanmalıyız,
- Tedaviyi anlayabilecek hastalarda;
- Ardışık-Birlikte (HİBRİD) tedavi ümit vericidir.
- PPI + Bizmut + A /14gün + (T + M /8-14 gün)
- Ardışık-Birlikte (HİBRİD) tedavi ümit vericidir.
[S146]
ÜÇLÜ TEDAVİ SONRASI SEMPTOMLARI KAYBOLAN ANCAK HELİKOBAKTER PİLORİ POZİTİFLİĞİ DEVAM EDEN ANTRAL GASTRİT HASTALARINDA EK TEDAVİ GEREKSİNİMİ
M. Manukyan*, U. Deveci*, A. Kebudi*, S. Kapaklı*, A. Midi**, N. Yener***Maltepe Üniversitesi Tıp Fakültesi Genel Cerrahi AD
**Maltepe Üniversitesi Tıp Fakültesi Patoloji AD
Amaç: Üçlü tedavi sonrası semptomları kaybolan ancak helikobakter pilori (Hp) pozitifliği devam eden hastalara ek tedavi gereksinimini ortaya koymak. Gereç ve yöntem: Kliniğimizde yapılan gastroskopilerinde yalnızca antral gastrit saptanan semptomatik 221 hastanın 158’inde biyopsi ile Hp pozitifliği gösterildi. Hp(+) hastalara amoksisilin 1 gr 2*1 klaritromisin 500mg 2*1 14 gün boyunca ve pantoprazol 40 mg iki ay boyunca verildi. Tedavi sonrası yapılan gaita analizlerinde 44 hastada Hp eradikasyonunun başarısız olduğu görüldü. Eradikasyonun başarısız olduğu bu hastalardan 32’si semptomlarının tümü ile yok olduğunu ifade etti. Asemptomatik hastalar iki gruba ayrıldı. Birinci gruptakilere tetrasiklin 4*500mg ve metranidazol 4*500mg’lık ikinci basamak tedavisi verildi. İkinci gruptaki hastalara sadece beslenme önerilerinde bulunuldu. Her iki grup hasta 6 ay sonra tekrar kontrole çağrıldı. Sonuçlar: Birinci gruptaki 16 hastanın gaitada Hp analizleri tekrarlandı. Sadece 6 hastada pozitifliğin devam ettiği ancak bu gruptaki 8 (dördü Hp-) hastada semptomların tekrar başladığı görüldü. Sadece diyet verilmiş olan ikinci gruptaki hastaların ise 7’si şikayetlerinin tekrarladığını ifade etti. Çıkarım:Antibiyotik tedavisi sonrası semptomları düzelen ancak Hp pozitifliği devam eden hastalarda Hp eradikasyonu amacı ile ikinci basamak tedavi vermenin klinik yararı yoktur.
Merhabalar… Bu yazımızda sizlere sıklıkla karşılaştığımız ve uygulama bazında çoğunlukla “alaylı” yaklaşımlar sergilediğimiz ( ‘’üçlü antibiyoterapisi yapıldı mı hastamızın?’’ ) açık kırıklar ve sonrasında gelişebilecek önemli komplikasyonlardan biri olan osteomiyelitlerle ilgili güncel bilgi ve öneriler paylaşılacaktır. Yazının kısa bir özetini de maddeler halinde yazının sonunda bulabilirsiniz. İyi okumalar…
Osteomiyelit inflamatuar hasarı takip eden yeni kemik oluşumu ile sonuçlanan kemiğin progresif bir enfeksiyonudur. Osteomiyelit Hipokrat zamanına kadar uzanan tarihteki en eski hastalıklardan biridir (M.Ö.460-370)(1) Nelaton, 1844 yılında osteomiyelit ismini bizlerle buluşturmadan önce ‘’medullada apse’’,’’nekroz’’,’’kemik iliğinin bir çıbanı ‘’ olarak tanımlanmakta idi. Penisilinin 1940 yılında dünya tıp tarihine girişiyle birlikte daha önceden sadece cerrahi tedavi yöntemleri kullanılan osteomiyelitte yeni bir çığır açılmış ve osteomiyelit kaynaklı sepsise bağlı yüksek mortalite oranları da düşüşe geçmiştir.
Osteomiyelitler hematojen yayılımla, komşuluk yoluyla ve vasküler yetmezlik ve diyabet gibi sistemik hastalıklar desteğinde oluşabilecekleri gibi posttravmatik olarak da meydana gelebilmektedirler. Hematojen osteomiyelitler çocuklarda erişkinlere göre daha sık görülmektedir ve çocuklarda uzun kemikler daha çok etkilenirken, bu süreç erişkinlerde vertebra olarak karşımıza çıkmaktadır (2). Komşuluk yoluyla oluşan osteomiyelitler daha genç bireylerde travma ve cerrahi sonrası meydana gelme eğilimindeyken, daha yaşlı erişkinlerde dekübit ülserler ve enfekte total eklem artroplastilerine sekonder olarak oluşma eğilimindedirler (3). Vasküler yetmezlik nedeniyle oluşan osteomiyelitler ise beklendiği üzere sıklıkla diyabetik hastalarda görülür.
Gelelim asıl konumuza. Posttravmatik osteomiyelitler, genellikle kontamine bir açık kırık veya kapalı kırıkların cerrahi tedavisi sonucu oluşan osteomiyelitlerdir. Posttravmatik osteomiyelitler açık kırıkların yüzde 25’ ine kadar görülebilmektedir ve bu risk aşağıdaki etkenlere bağlıdır: (4-9)
- Fraktürün ciddiyeti
- Yumuşak doku yaralanmasının ciddiyeti
- Bakteriyel kontaminasyonun derecesi
- Altta yatan vasküler yetmezlik mevcudiyeti (periferik vasküler hastalık veya diyabet )
- Cerrahi debridmanın yeterliliği
Mikroorganizmalar travma sırasında doğrudan kemiğe ulaşabileceği gibi üstteki yumuşak doku hasarından komşuluk yoluyla da yayılabilir. Pıhtılaşmış kan ve nekrotik kemik gibi devitalize dokuların mevcudiyetinde ise daha kolay çoğalırlar. Posttravmatik osteomiyelit patojenleri cilt florasını, topraktaki organizmaları veya hastanede cerrahi müdahale sırası, sonrası veya öncesinde edinilen nazokomiyal patojenleri içerir. Staphylococcus aureus, koagülaz negatif stafilokoklar ve aerobik gram negatif basiller en sık görülen mikroorganizmalar olsalar da; enterokoklar, anaeroblar, mantarlar ve mikobakteriler da etken olarak karşımıza çıkmaktadırlar (1,6,10-15). Benzer mikrobiyoloji çocuklarda da görülmektedir (16-17).
Bunların yanında tibial fraktürü olan savaş yaralılarındaki yara enfeksiyonları ile Acinetobacter baumannii ve Pseudomonas aeruginosa’nın aralarında bulunduğu ilaç dirençli aerobik gram negatif organizmalar ilişkilendirilmiştir (18).
Osteomiyelit geliştiği zaman ilk debridmanda alınan kültürler her zaman sorumlu patojeni yansıtmazlar ve aralarındaki korelasyon yaklaşık %25’tir (19-20).Bu durumun sebebi ise yaralanma anında yarada kolonize olan mikroorganizmaların kemik dokusunda o anda enfeksiyon yapamazken, ilk yaralanmada mevcut olmayan patojenlerin daha sonradan kolonize olarak yarayı enfekte edebilmeleridir.
Posttravmatik osteomiyelitin temel işaretleri; kırık bölgesinde birleşmenin olmaması ve yara kapatılması sonrası zayıf yara iyileşmesidir. Diğer semptomlar ateş, lokal yara drenajı, eritem, ısı artışı, şişlik ve ağrıdan oluşur.
Sınırlı kan desteği ve kendisini çevreleyen kas dokusunun azlığı nedeniyle tibia postravmatik osteomiyelitten en sık etkilenen kemiktir (10,21,22)
Açık Kırık Sınıflandırması
Açık kırıklar Gustillo-Anderson sistemine göre değerlendirilirler; bu değerlendirme intraoperatif yapılabileceği gibi, ilk muayene sırasında da bu sisteme göre değerlendirilebilir. Açık kırık derecesinde artış; artan enfeksiyon riski ve amputasyon oranı ile ilişkilidir (27,28). Bu skorlama sisteminin bir dezavantajı gözlemciler arasındaki düşük uyum oranıdır (%60).
GUSTILLO – ANDERSON SİSTEMİ
TİP 1: Yara < 1 cm; minimal kontaminasyon,ezilme veya yumuşak doku hasarı
TİP 2: Yara >1 cm ; orta derecede yumuşak doku hasarı; minimal periostal soyulma
TİP 3A: Ciddi doku hasarı ve bol miktarda kontaminasyon; yara cilt dokusuyla kapanabiliyor
TİP 3B: Ciddi doku hasarı ve bol miktarda kontaminasyon; yara cilt dokusuyla kapanamıyor
TİP 3C: Onarım gerektiren arter yaralanmalı açık fraktür
Açık Kırıklara Yaklaşım
İlk müdahale irrigasyon ve debridmandan oluşmaktadır. Yeterli miktarda yapılan irrigasyon, yara yerindeki yabancı cisimleri de temizleyerek enfeksiyon gelişimini engelleyen en önemli parametredir. Kemik biyopsileri veya nekrotik dokunun yüzeyel debridmanı sırasında edinilen sıvı koleksiyonlarının rutin kültürlerinin alınmasına gerek yoktur. Şüpheli enfeksiyon için tekrar kültür alındığında aerobik ve anaerobik kültür alınmalıdır. Antibiyotik ve tetanoz immunizasyonu mutlaka yapılmalıdır (23).
Açık yaralanma sonrası 6 saat içinde parenteral antibiyotiklerin uygulanması yumuşak doku enfeksiyonu veya osteomiyelit riskini azaltmak için gereklidir (21,23-25).
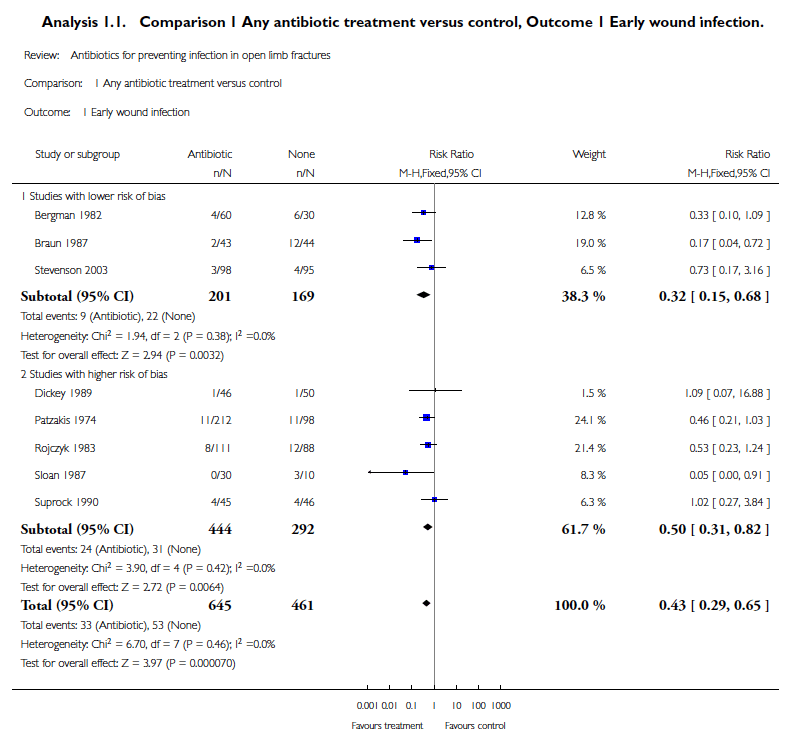
Antibiyotik tedavisi yara debridmanı sırasında da yapılmalıdır. Antibiyotik tedavisinin süresi fraktürün sınıflandırılma derecesine bağlıdır. Kapalı kırıklar için tek doz antibiyotik cerrahi onarım sırasında yeterlidir. En son 2004 yılında yapılan bir Cochrane derlemesine göre, açık kırıklarda antibiyotik uygulaması yara yeri enfeksiyonu gelişimini yarı yarıya azaltmaktadır (risk oranı %43). Bu derlemeyle ilgili tartışmaya aşağıdaki editoryal nottan ulaşabilirsiniz.
Peki tedavi için antibiyotik önerileri nelerdir?
Medscape:
- Tip 1 yaralanmalar için SEFAZOLİN veya eş değeri gram pozitiflere karşı etkin bir antibiyoterapi başlanmalı
- Tip 2 veya 3 yaralanmalı hastalar için aminoglikozitler gibi gram negatif kapsamlı bir antibiyoterapi mevcut tedaviye eklenmeli
- Anaerobik enfeksiyon riski taşıyan yaralar için penisilin veya klindamisin eklenebilir.
Up To Date:
- İlk ampirik parenteral antibiyotik tedavisi gram pozitif ve gram negatif organizmalara karşı olmalıdır. Bu spektrumu kapsaması açısından SEFUROKSİM uygundur .
- MRSA şüphesinde MRSA’ya etkin VANKOMİSİN gibi antibiyotikler tedaviye eklenmelidir.
- Sefalosporinlerin kullanılamadığı durumlarda florokinolonlar gram negatif aktivitesi ile alternatif bir profilaktik ajan sınıfıdır. Kemik dokusuna yüksek penetrasyon gösterirler(Sefuroksim 0,04-0,55,levofloksasin 0,36-1-ortalama kemik/serum konsantrasyon oranları)
En son 2011 yılında güncellenen East Practice Management Group’un sistematik derlemesinin sonuçlarına göre tip 1 ve tip 2 yaralanmalarda sadece gram pozitiflere etkili bir antibiyotik uygulanması (örn. sefazolin), tip 3 yaralanmalarda ise buna bir aminoglikozid eklenmesi gerektiğinden bahsetmektedir (ör. gentamisin). Tip 2 fraktürlerde de aminoglikozid kullanılmasıyla ilgili daha düşük kanıt düzeyinden öneri de bulunmaktadır. Buna göre literatürde birçok farklı tedavi önerileri bulunsa da genel görüş aşağıdaki şekilde karşımıza çıkmakta:
- Tip 1 :Birinci kuşak sefalosporin (sefazolin)
- Tip 2 ve 3 : Birinci kuşak sefalosporin + aminoglikozit
- Yaranın özelliği göz önüne alınarak olası mikroorganizmalara yönelik tedavi eklenebilir (toprak ile kontamine yara için penisilin/metranidazol gibi)
Tedavi süresi ne kadar olmalı ?
Kesin bir görüş yok.
Gustillo – Anderson tip 1 açık kırıklar için 24-48, tip 2 ve 3 açık kırıklar içinse 48-72 saat profilaktik antibiyotik kullanımı gereklidir. Profilaktik antibiyotiklerin uzamış kullanımı enfeksiyon riskini azaltmadığı gibi dirençli organizmaların oluşumuna da neden olabilmektedir (23,29).
AKLIMIZDA KALMASI GEREKENLER
- Açık kırıklarda ilk 3 saatte uygulanan antibiyoterapi enfeksiyon riskini oldukça azaltmaktadır (7).
- Posttravmatik osteomiyelitler açık kırıkların yüzde 25’ine kadar görülebilmektedir.
- Sınırlı kan desteği ve kendisini çevreleyen kas dokusunun azlığı nedeniyle tibia postravmatik osteomiyelitten en sık etkilenen kemiktir (10,21,22).
- Gustillo-Anderson sınıflaması hastanın ilk muayenesinde de değerlendirilebilecek bir sınıflamadır ve açık kırık derecesinde artış, artan enfeksiyon riski ve amputasyon oranı ile ilişkilidir (27,28).
- Kemik biyopsileri veya nekrotik dokunun yüzeyel debridmanı sırasında edinilen sıvı koleksiyonlarının rutin kültürlerinin alınmasına gerek yoktur. Osteomiyelit geliştiği zaman ilk debridmanda alınan kültürler her zaman sorumlu patojeni yansıtmazlar ve aralarındaki korelasyon yaklaşık %25’tir (19-20).
- Tedavi protokolü aşağıdaki gibi olabilir:
- Tip 1 :Birinci kuşak sefalosporin (sefazolin )
- Tip 2 ve 3 : Birinci kuşak sefalosporin + aminoglikozit(tobramisin,gentamisin)
- Yaranın özelliği göz önüne alınarak olası mikroorganizmalara yönelik tedavi eklenebilir (toprak ile kontamine yara için penisilin/metranidazol gibi)
Bir sonraki yazımızda tekrar görüşmek umuduyla…
Editör Notu:
Açık kırıkların yönetimiyle ilgili daha yüksek kanıt düzeyine sahip yazılara sahip olmamız gerektiği açık. Antibiyoterapinin plaseboya üstünlüğünü çalışan Cochrane derlemesindeki verilerle; antibiyoterapiyle absolut risk azalması ne kadar peki diye hesapladığımızda bu oranın %6.3 olduğunu görüyoruz, bunu NNT değeri olarak ifade edersek bu sayı da 16. Yani açık kırıklarda antibiyoterapiden her 16 hastadan biri fayda görüyor. Bu NNT değerinden alınması gereken mesaj şu; proflaktik antibiyoterapiyi hiç şüphesiz bu hastalara uygulayalım, ama muhtemelen bu hastalarda infeksiyon gelişimini belirleyen daha güçlü parametreler de var. Uygun yara yeri temizliği yapılmamış, debridman uygulanmamış kirli bir yaraya hangi antibiyotiği uygularsanız uygulayın sonuç yüz güldürücü olmayabilir.
Antibiyotik seçimiyle ilgili kanıtlar oldukça az, bunun nedeni de ortopedi literatüründe bunu spesifik kemik kırıkları için ayrı ayrı çalışılmış olması. Gustillo-Anderson tip 1 kırıklara “üçlü” antibiyotik uygulamanın anlamsız olduğu çok açık. Benzer şekilde tip 2 kırıklarda da antibiyotik seçiminin hasta bazında özelleştirilmesi gerekiyor, her hastaya aminoglikozid eklemek uygun olmayabilir. Mantıklı olan; kırığın tipinin, oluşum mekanizmasının, kirlilik derecesinin ve hastanın altta yatan hastalıklarının göz önüne alınarak tedavinin hasta bazında özelleştirilmesi.
Editör: Dr. Nurettin Özgür DOĞAN
Kaynaklar
- Lew DP, Waldvogel FA. Osteomyelitis. Lancet 2004; 364:369.
- David R, Barron BJ, Madewell JE. Osteomyelitis, acute and chronic. Radiol Clin North Am 1987; 25:1171.
- Waldvogel FA, Medoff G, Swartz MN. Osteomyelitis: a review of clinical features, therapeutic considerations and unusual aspects. N Engl J Med 1970; 282:198.
- Merritt K. Factors increasing the risk of infection in patients with open fractures. J Trauma 1988; 28:823.
- DeLong WG Jr, Born CT, Wei SY, et al. Aggressive treatment of 119 open fracture wounds. J Trauma 1999; 46:1049.
- Gross T, Kaim AH, Regazzoni P, Widmer AF. Current concepts in posttraumatic osteomyelitis: a diagnostic challenge with new imaging options. J Trauma 2002; 52:1210.
- Patzakis MJ, Wilkins J. Factors influencing infection rate in open fracture wounds. Clin Orthop Relat Res 1989; :36.
- Tsukayama DT. Pathophysiology of posttraumatic osteomyelitis. Clin Orthop Relat Res 1999; :22.
- Lavery LA, Walker SC, Harkless LB, Felder-Johnson K. Infected puncture wounds in diabetic and nondiabetic adults. Diabetes Care 1995; 18:1588.
- Khatod M, Botte MJ, Hoyt DB, et al. Outcomes in open tibia fractures: relationship between delay in treatment and infection. J Trauma 2003; 55:949.
- Mader JT, Ortiz M, Calhoun JH. Update on the diagnosis and management of osteomyelitis. Clin Podiatr Med Surg 1996; 13:701.
- Trampuz A, Zimmerli W. Diagnosis and treatment of infections associated with fracture-fixation devices. Injury 2006; 37 Suppl 2:S59.
- Haas DW, McAndrew MP. Bacterial osteomyelitis in adults: evolving considerations in diagnosis and treatment. Am J Med 1996; 101:550.
- Karam GH, Ackley AM, Dismukes WE. Posttraumatic Aeromonas hydrophila osteomyelitis. Arch Intern Med 1983; 143:2073.
- Lavery LA, Harkless LB, Felder-Johnson K, Mundine S. Bacterial pathogens in infected puncture wounds in adults with diabetes. J Foot Ankle Surg 1994; 33:91.
- Laughlin TJ, Armstrong DG, Caporusso J, Lavery LA. Soft tissue and bone infections from puncture wounds in children. West J Med 1997; 166:126.
- Harkness B, Andresen D, Kesson A, Isaacs D. Infections following lawnmower and farm machinery-related injuries in children. J Paediatr Child Health 2009; 45:525.
- Johnson EN, Burns TC, Hayda RA, et al. Infectious complications of open type III tibial fractures among combat casualties. Clin Infect Dis 2007; 45:409.
- Kindsfater K, Jonassen EA. Osteomyelitis in grade II and III open tibia fractures with late debridement. J Orthop Trauma 1995; 9:121.
- Lee J. Efficacy of cultures in the management of open fractures. Clin Orthop Relat Res 1997; :71.
- Patzakis MJ, Wilkins J, Moore TM. Considerations in reducing the infection rate in open tibial fractures. Clin Orthop Relat Res 1983; :36.
- Mader JT, Cripps MW, Calhoun JH. Adult posttraumatic osteomyelitis of the tibia. Clin Orthop Relat Res 1999; :14.
- Eastern Association for the Surgery of Trauma (EAST) working group. Practice management guidelines for prophylactic antibiotic use in open fractures, 2011 update
- Seligson D, Henry SL. Treatment of compound fractures. Am J Surg 1991; 161:693.
- Patzakis MJ, Bains RS, Lee J, et al. Prospective, randomized, double-blind study comparing single-agent antibiotic therapy, ciprofloxacin, to combination antibiotic therapy in open fracture wounds. J Orthop Trauma 2000; 14:529.
- Gosselin RA, Roberts I, Gillespie WJ. Antibiotics for preventing infection in open limb fractures. Cochrane Database Syst Rev 2004; :CD003764.
- Gustilo RB, Mendoza RM, Williams DN. Problems in the management of type III (severe) open fractures: a new classification of type III open fractures. J Trauma 1984; 24:742.
- Gustilo RB, Anderson JT. Prevention of infection in the treatment of one thousand and twenty-five open fractures of long bones: retrospective and prospective analyses. J Bone Joint Surg Am 1976; 58:453.
- Dellinger EP, Caplan ES, Weaver LD, et al. Duration of preventive antibiotic administration for open extremity fractures. Arch Surg 1988; 123:333.